HPPでは、酵素の欠損が骨・全身・生命に影響を及ぼします1-7
ALPの活性低下が低ホスファターゼ症(HPP)の原因です1,8,9
酵素であるアルカリフォスファターゼ(ALP)の欠損、またはALPの活性低下が、HPPに関連する症状や早期死亡の原因です1,8,9
ALPの活性低下は、ALPL遺伝子の変異によって起こります。この欠損によりALPの基質が蓄積し、衰弱性または生命を脅かす症状の原因となります1,8-13
多くの遺伝性疾患と同様に、HPPにおいても基礎にある生化学的異常と病理過程は生涯にわたって続きますが、症状が現れない場合や、後年まで症状が認められない場合もあります1
ALPは、体内において、次の3つの基質の代謝に重要な役割を担っています9,11
- ピリドキサール5ʹ-リン酸(PLPまたはビタミンB6)
- 無機ピロリン酸(PPi)
- フォスフォエタノールアミン(PEA)
PEA高値はHPPの診断マーカーとなっていますが、その病理学的意義はまだ十分に解明されていません1,8,9
※PPi、PLPは、現在日本では測定できません
疾患のメカニズム(MOD)のビデオを見る
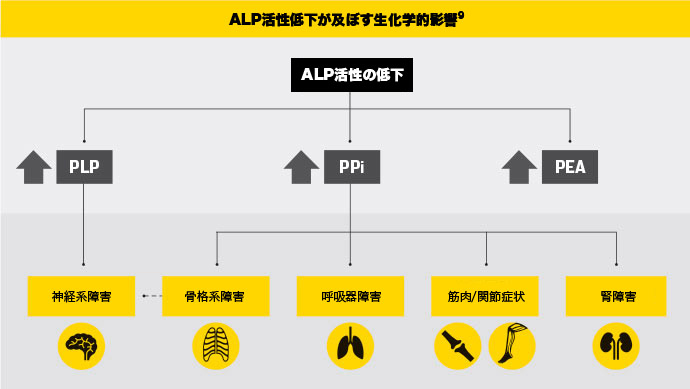
ALP活性低下とその結果生じる生化学的異常が、全身性疾患の病理につながります
PLP
活性型ビタミンB6であるPLPは、ALP活性の低下により全身に蓄積します。ビタミンB6は、ALPによって脱リン酸化されないと脳内の中枢神経系に入ることができないため、脳内ではPLPが欠損しビタミンB6依存性けいれん発作を引き起こします。これら神経系への影響は、頭蓋骨縫合早期癒合症と脳脊髄液(CSF)圧の上昇によって悪化します4,8,9,14,15
PPi
PPiは、骨石灰化に対する天然の阻害物質です。ALPの低下が著しい場合には、PPiが蓄積して、骨石灰化を阻害するため、骨形成、骨の安定性、骨へのカルシウム沈着が著しく妨げられます。これによって、特徴的な骨格系および全身性の病態を引き起こします8,16:
- 非外傷性の骨折を繰り返し、体が衰弱し、骨折が十分に治癒しません8,17,18
- カルシウムの血清および尿中濃度の上昇に伴い、腎石灰化が生じ、腎不全に進行する可能性があります3,19,20
- 頭蓋骨縫合早期癒合症により、CSF圧の上昇とけいれん発作が生じます8,14
- 肋骨の重度の低石灰化により、肺低形成と呼吸不全を引き起こすことがあります8,21
- ピロリン酸カルシウム二水和物(CPPD)の結晶の沈着や、慢性の疼痛と炎症を伴う関節症状が生じます8,22,23
PEA
PEAは、特定のリン脂質の形成に用いられるアミノ酸誘導体です。PEAの蓄積はHPPの診断マーカーですが、その病理学的意義は十分に解明されていません8,9
PPiとPLPの蓄積によって、衰弱性または生命を脅かす骨格系や全身性の症状を引き起こします1,4,8,9,14-16
HPPの重篤な症状
References: 1. Rockman-Greenberg C. Hypophosphatasia. Pediatr Endocrinol Rev. 2013;10(suppl 2):380-388. 2. Baumgartner-Sigl S, Haberlandt E, Mumm S, et al. Pyridoxine-responsive seizures as the first symptom of infantile hypophosphatasia caused by two novel missense mutations (c.677T>C, p.M226T; c.1112C>T, p.T371I) of the tissue-nonspecific alkaline phosphatase gene. Bone. 2007;40(6):1655-1661. 3. Eade AWT, Swannell AJ, Williamson N. Pyrophosphate arthropathy in hypophosphatasia. Ann Rheum Dis. 1981;40(2):164-170. 4. Balasubramaniam S, Bowling F, Carpenter K, et al. Perinatal hypophosphatasia presenting as neonatal epileptic encephalopathy with abnormal neurotransmitter metabolism secondary to reduced co-factor pyridoxal-5-phosphate availability. J Inherit Metab Dis. 2010;33(3):25-33. 5. Seshia SS, Derbyshire G, Haworth JC, Hoogstraten J. Myopathy with hypophosphatasia. Arch Dis Child. 1990;65(1):130-131. 6. Whyte MP, Murphy WA, Fallon MD. Adult hypophosphatasia with chondrocalcinosis and arthropathy: variable penetrance of hypophosphatasemia in a large Oklahoma kindred. Am J Med. 1982;72(4):631-641. 7. Fallon MD, Teitelbaum SL, Weinstein RS, Goldfischer S, Brown DM, Whyte MP. Hypophosphatasia: clinicopathologic comparison of the infantile, childhood, and adult forms. Medicine. 1984;63(1):12-24. 8. Whyte MP. Hypophosphatasia: nature’s window on alkaline phosphatase function in humans. In: Bilezikian JP, Raisz LG, Martin TJ, eds. Principles of Bone Biology. Vol 1. 3rd ed. San Diego, CA: Academic Press; 2008:1573-1598. 9. Whyte MP. Hypophosphatasia. In: Scriver CR, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Bases of Inherited Disease. Vol 4. 8th ed. New York, NY: McGraw-Hill; 2001:5313-5329. 10. Fraser D. Hypophosphatasia. Am J Med. 1957;22(5):730-746. 11. Mornet E, Nunes ME. Hypophosphatasia. In: Pagon RA, Bird TD, Dolan CR, Stephen K, eds. GeneReviews. Seattle, WA: University of Washington, Seattle; 1993. http://www.ncbi.nlm.nih.gov/books/NBK1150/. Published November 20, 2007. Updated August 5, 2010. Accessed March 31, 2014. 12. Whyte MP, Mahuren JD, Vrabel LA, Coburn SP. Markedly increased circulating pyridoxal-5’-phosphate levels in hypophosphatasia. J Clin Invest. 1985;76(2):752-756. 13. Greenberg CR, Taylor CLD, Haworth JC, et al. A homoallelic Gly317 → Asp mutation in ALPL causes the perinatal (lethal) form of hypophosphatasia in Canadian Mennonites. Genomics. 1993;17(1):215-217. 14. Collmann H, Mornet E, Gattenlöhner S, Beck C, Girschick H. Neurosurgical aspects of childhood hypophosphatasia. Childs Nerv Syst. 2009;25(2):217-223. 15. Plecko B, Stöckler B. Vitamin B6 dependent seizures. Can J Neurol Sci. 2009;36(2):S73-S77. 16. Anderson HC, Hsu HH, Morris DC, Fedde KN, Whyte MP. Matrix vesicles in osteomalacic hypophosphatasia bone contain apatite-like mineral crystals. Am J Pathol. 1997;151(6):1555-1561. 17. Moulin P, Vaysse F, Bieth E, et al. Hypophosphatasia may lead to bone fragility: don’t miss it. Eur J Pediatr. 2009;168(7):783-788. 18. Coe JD, Murphy WA, Whyte MP. Management of femoral fractures and pseudofractures in adult hypophosphatasia. J Bone Joint Surg Am. 1986;68(7):981-990. 19. Caswell AM, Whyte MP, Russell RGG. Hypophosphatasia and the extracellular metabolism of inorganic pyrophosphate: clinical and laboratory aspects. Crit Rev Clin Lab Sci. 1991;28(3):175-232. 20. Mohn A, De Leonibus C, de Giorgis T, Mornet E, Chiarelli F. Hypophosphatasia in a child with widened anterior fontanelle: lessons learned from late diagnosis and incorrect treatment. Acta Paediatr. 2011;100(7):e43-e46. 21. Silver MM, Vilos GA. Pulmonary hypoplasia in neonatal hypophosphatasia. Pediatr Pathol. 1988;8(5):483-493. 22. Beck C, Morbach H, Richl P, Stenzel M, Girschick HJ. How can calcium pyrophosphate crystals induce inflammation in hypophosphatasia or chronic inflammatory joint diseases? Rheumatol Int. 2009;29(3):229-238. 23. Chuck AJ, Pattrick MG, Hamilton E, Wilson R, Doherty M. Crystal deposition in hypophosphatasia: a reappraisal. Ann Rheum Dis. 1989;48(7):571-576.


